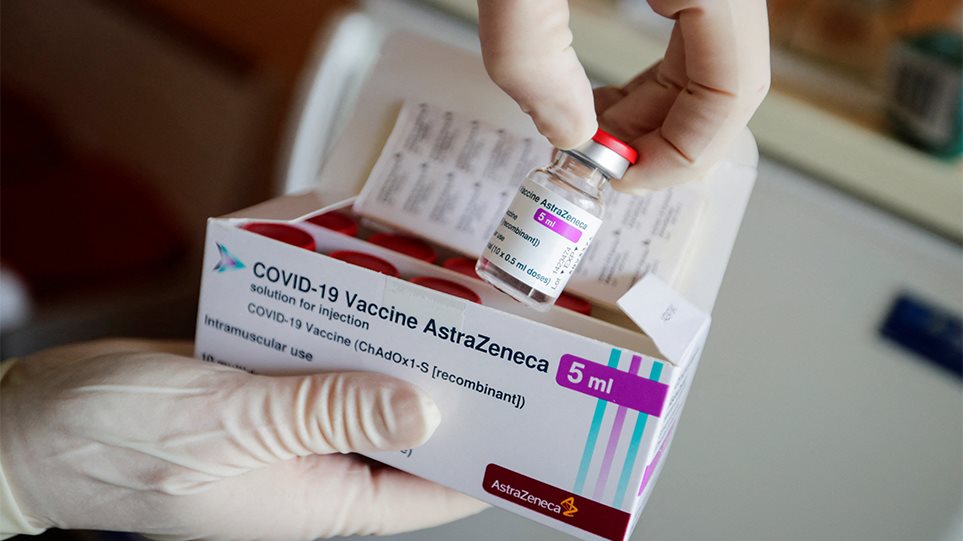
Συνεδριάζει η Επιτροπή Εμβολιασμών – Θα προχωρήσει και η Ελλάδα σε αποκλεισμό συγκεκριμένων ηλικιών από τον εμβολιασμό με AstaZeneca; – «Βαβέλ» η ΕΕ: Χωρίς κοινή θέση για τα όρια ηλικίας
Αποφάσεις αναμένονται σχετικά με το εμβόλιο της AstraZeneca στην χώρα μας, καθώς αύριο συνεδριάζει η Εθνική Επιτροπή Εμβολιασμών.
Υπενθυμίζεται πως χθες, ο Ευρωπαϊκός Οργανισμός Φαρμάκων κατέληξε στο συμπέρασμα ότι οι ασυνήθιστοι θρόμβοι στο αίμα σε συνδυασμό με χαμηλά αιμοπετάλια, θα πρέπει να αναφέρονται ως πολύ σπάνιες ανεπιθύμητες ενέργειες του συγκεκριμένου εμβολίου. Της απόφασης αυτής, ωστόσο δεν ακολούθησε μία ενιαία θέση της Ευρωπαϊκής Ένωσης με τις χώρες να επιλέγουν διαφορετική προσέγγιση στο θέμα.
Σύμφωνα λοιπόν με τις πληροφορίες του protothema.gr
ανάμεσα σε αυτά που εξετάζεται είναι ένας τρόπος προκειμένου αφενός να μην χαθούν δόσεις και αφετέρου να επιταχυνθεί η εμβολιαστική διαδικασία δίνοντας την δυνατότητα σε πολίτες που δεν έχουν αντίρρηση να κάνουν το εμβόλιο της AstraZeneca να συμμετάσχουν στον εμβολιασμό νωρίτερα.
Για να επιτευχθεί κάτι τέτοιο θα πρέπει λοιπόν να «ανοίξει» η πλατφόρμα τόσο για άλλες ηλικιακές ομάδες όσο και για συγκεκριμένες επαγγελματικές κατηγορίες, ενόψει και της επανεκκίνησης των οικονομικών δραστηριοτήτων.
Την ίδια ώρα σύμφωνα με τις πληροφορίες του protothema.gr στο τραπέζι βρίσκεται και ο αποκλεισμός συγκεκριμένων ηλικιών από τον εμβολιασμό με το σκεύασμα της AstraZeneca προκειμένου να ελαχιστοποιηθεί η πιθανότητα παρενεργειών, μία επιλογή που έχουν κάνει άλλες χώρες όπως η Μεγάλη Βρετανία και η Γερμανία.
«Βαβέλ» η ΕΕ – Χωρίς κοινή θέση για τα όρια ηλικίας
Διαφορετικές προσεγγίσεις αναφορικά με τη χρήση του εμβολίου της AstraZeneca (το οποίο πλέον ονομάζεται Vaxzevria), τόσο στον γενικό πληθυσμό όσο και σε συγκεκριμένες ηλικιακές ομάδες, καταγράφονται στα κράτη-μέλη της Ευρωπαϊκής Ένωσης. Παρόλο που ο Ευρωπαϊκός Οργανισμός Φαρμάκων κατέληξε στο συμπέρασμα ότι οι ασυνήθιστοι θρόμβοι στο αίμα σε συνδυασμό με χαμηλά αιμοπετάλια, θα πρέπει να αναφέρονται ως πολύ σπάνιες ανεπιθύμητες ενέργειες του εμβολίου, τα οφέλη του οποίου είναι περισσότερα από πιθανούς κινδύνους, οι 27 υπουργοί Υγείας δεν κατάφεραν να καταλήξουν σε μια κοινή θέση.
Η επιτροπή ασφάλειας και φαρμακοεπαγρύπνησης του Ευρωπαϊκού Οργανισμού Φαρμάκων (ΕΜΑ) επιβεβαίωσε χθες, Τετάρτη 7 Απριλίου, ότι οι «ασυνήθιστες θρομβώσεις με χαμηλά αιμοπετάλια πρέπει να καταχωρηθούν ως πιθανή παρενέργεια» του συγκεκριμένου εμβολίου, ωστόσο συνέστησε στα κράτη – μέλη να συνεχίσουν το πρόγραμμα εμβολιασμού, καθώς όλα τα εμβόλια είναι απαραίτητα στη μάχη κατά της Covid-19. Παράλληλα ο ΕΜΑ υπενθύμισε στους επαγγελματίες του τομέα της υγείας και σε άτομα που λαμβάνουν το εμβόλιο να παραμένουν ενήμεροι για την πιθανότητα εμφάνισης πολύ σπανίων περιπτώσεων θρόμβων αίματος σε συνδυασμό με τα χαμηλά επίπεδα αιμοπεταλίων, εντός 2 εβδομάδων από τον εμβολιασμό.
Μέχρι στιγμής, οι περισσότερες από τις αναφερόμενες περιπτώσεις έχουν συμβεί σε γυναίκες κάτω των 60 ετών εντός 2 εβδομάδων από τον εμβολιασμό. Με βάση τα διαθέσιμα στοιχεία, συγκεκριμένοι παράγοντες κινδύνου, όπως η ηλικία, το φύλο ή προϋπάρχουσες παθήσεις, δεν έχουν επιβεβαιωθεί. Επιπλέον, η επιτροπή του ΕΜΑ ανέφερε πως τα άτομα που έχουν λάβει το εμβόλιο θα πρέπει να ζητήσουν ιατρική βοήθεια αμέσως εάν εμφανίσουν συμπτώματα αυτού του συνδυασμού θρόμβων αίματος και χαμηλών αιμοπεταλίων.
Η επιτροπή του ΕΜΑ διενήργησε εμπεριστατωμένη ανασκόπηση 62 περιπτώσεων εγκεφαλικής θρόμβωσης και 24 περιπτώσεων θρόμβωσης πυλαίας φλέβας που αναφέρθηκαν σε βάση δεδομένων ασφάλειας της ΕΕ (EudraVigilance) για τα φάρμακα μέχρι τις 22 Μαρτίου, 18 εκ των οποίων ήταν θανατηφόρες. Τα περιστατικά προήλθαν κυρίως από συστήματα αναφοράς του ΕΜΑ και του Ηνωμένου Βασιλείου, όπου περίπου 25 εκατομμύρια άνθρωποι είχαν λάβει το συγκεκριμένο εμβόλιο.
Ωστόσο οι 27 υπουργοί Υγείας της Ευρωπαϊκής Ένωσης κατά την έκτακτη τηλεδιάσκεψη που πραγματοποίησαν, μετά τις ανακοινώσεις του ΕΜΑ, δεν κατάφεραν να συμφωνήσουν σε μια κοινή θέση και οι συνομιλίες αναμένεται να συνεχιστούν τις επόμενες ημέρες. Η πορτογαλική προεδρία του Συμβουλίου της ΕΕ κάλεσε τους υπουργούς Υγείας να συντονίσουν τις ενέργειές τους καθώς το ζήτημα του εμβολίου της AstraZeneca «ενδέχεται να έχει άμεσο αντίκτυπο όχι μόνο στα εθνικά σχέδια εμβολιασμού, αλλά και στην εμπιστοσύνη των πολιτών μας στα εμβόλια κατά της Covid-19».
Ωστόσο, τα κράτη – μέλη της ΕΕ συνεχίζουν να προτείνουν διαφορετικά όρια ηλικίας για τη χρήση του εμβολίου, παρόλο που ο EMA υπογράμμισε ότι δεν υπάρχουν δεδομένα που να δικαιολογούν μια τέτοια απόφαση.
Η Γερμανία έχει ορίσει ότι το σκεύασμα της αγγλο-σουηδικής φαρμακευτικής θα χορηγείται σε πολίτες άνω των 60 ετών και σε ομάδες υψηλής προτεραιότητας, ενώ η αρμόδια επιτροπή ελέγχου των εμβολιασμών προτείνει σε όσους είναι κάτω των 60 χρόνων και έχουν λάβει την πρώτη δόση του εμβολίου της AstraZeneca να εμβολιαστούν με διαφορετικό σκεύασμα την δεύτερη φορά.
Η Γαλλία και το Βέλγιο δήλωσαν ότι το εμβόλιο πρέπει να χορηγείται μόνο σε πολίτες ηλικίας 55 ετών και άνω. Στη Φινλανδία χορηγείται μόνο σε άτομα ηλικίας 65 ετών και άνω, ενώ στην Εσθονία σε πολίτες άνω των 60 ετών. Στην Ισπανία, ορισμένες περιοχές της χώρας, όπως η Καστίλλη και η Λεόν, ανέστειλαν εκ νέου τους εμβολιασμούς με τον εν λόγω σκεύασμα και στη συνέχεια η κυβέρνηση της χώρας ανακοίνωσε ότι το εμβόλιο θα χορηγείται σε πολίτες άνω των 60 ετών.
Η ΕΕ προσπαθεί να επιταχύνει την παραγωγή εμβολίων σε ευρωπαϊκό έδαφος
Παρόλα τα προβλήματα που έχουν προκύψει με την AstraZeneca, η ΕΕ βασίζεται στην προμήθεια τεραστίων ποσοτήτων εμβολίων κατά το δεύτερο τρίμηνο του έτους. Μέσα στους επόμενους τρεις μήνες η ΕΕ θα έχει στη διάθεσή της περισσότερες από 360 εκατ. δόσεις που θα προστεθούν στις περίπου 170 εκατ. που έχει παραλάβει ήδη.
Σε μια προσπάθεια ενίσχυσης της παραγωγής σε ευρωπαϊκό έδαφος ο Ευρωπαϊκός Οργανισμός Φαρμάκων (EMA) ενέκρινε πρόσφατα νέους χώρους παραγωγής των εμβολίων των BioNTech-Pfizer και της Moderna, στην Ολλανδία, τη Γερμανία και την Ελβετία. Συγκεκριμένα οι πρώτες παραδόσεις του εμβολίου BioNTech-Pfizer που κατασκευάζονται στο Μαρβούργο, στο κρατίδιο της Έσσης, έχουν προγραμματιστεί για το δεύτερο μισό του Απριλίου. Η BioNTech αναφέρει ότι σχεδιάζει να παράγει έως και 250 εκατ. δόσεις του εμβολίου της κατά το πρώτο εξάμηνο του έτους.
Παράλληλα, ορισμένοι κατασκευαστές εμβολίων όπως η γερμανική CureVac, υποστηρίζουν ότι αντιμετωπίζουν προκλήσεις στην αύξηση της παραγωγής στην Ευρώπη, λόγω της απόφασης της προηγούμενης κυβέρνησης των ΗΠΑ να απαγορεύσει τις εξαγωγές που σχετίζονται με τα εμβόλια, με σκοπό να καλύψει τις ανάγκες των Αμερικανών πολιτών. Σύμφωνα με εκπροσώπους της CureVac, το εμβόλιο της που βασίζεται στην «τεχνολογία του m-RNA», θα μπορούσε να λάβει έκτακτη έγκριση από τον ΕΜΑ μέσα στις επόμενες εβδομάδες και η εταιρεία θα μπορούσε να παρασκευάσει 300 εκατ. δόσεις μέσα στους επόμενους μήνες.